

2020年5月19日,国家药监局综合司发布关于2020年医疗器械行业标准制修订计划项目通知,其中《医疗器械体外皮肤刺激试验》项目由山东省医疗器械产品质量检验中心、北京市医疗器械检验所、中国食品药品检定研究院、济南磐升生物技术有限公司共同起草制定。此项标准制定是为了保证医疗器械在人体上使用的安全性。ISO10993《医疗器械生物学评价》系列标准中规定了一系列医疗器械生物学评价指导性方法,我国将其转化成为GB/T16886《医疗器械生物学评价》系列标准。该标准的主要目的是保护人体使用安全,另一重要的目的是保护动物,使实验室动物使用数量和试验次数减少的到最低量。
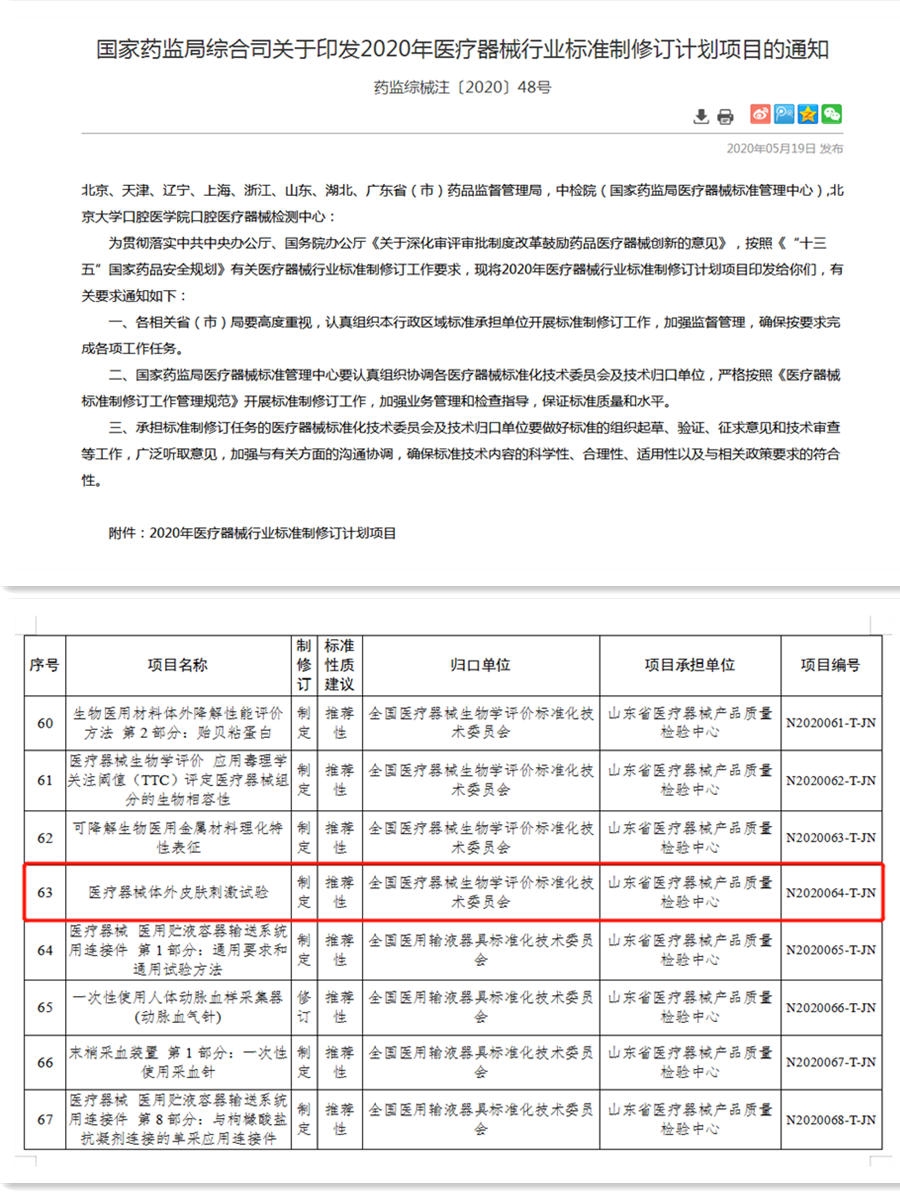
目前GB/T 16886《医疗器械生物学评价》第5部分已经明确规定了医疗器械在注册审批前需要进行体外细胞毒性试验。这一规定大大减少了医疗器械产品的动物使用量。而对于医疗器械产品的皮肤刺激性和致敏性仍旧采用的是动物实验。为了改变这一现状,山东省医疗器械产品质量检验中心、北京市医疗器械检验所、中国食品药品检定研究院、济南磐升生物技术有限公司合作开展3D人表皮模型医疗器械产品的皮肤刺激性测试的方法学验证工作。
磐升生物研发的3D人表皮模型即人工表皮检测试剂盒,是一种以来源于健康中国人的表皮角质形成细胞为种子细胞,通过体外培养而获得的高度分化、分层的三维表皮模型。广泛用于化妆品、化学品、药品、医疗器械以及纺织品等的体外检测。传统的动物实验不仅给动物造成痛苦,检测成本高,而且由于动物和人皮肤的结构和功能的差异,很难推断动物实验结果应用于人体的安全性。而磐升生物研发的人工表皮检测试剂盒用于体外皮肤刺激性检测,不仅能有效节省成本,还促进了体外替代技术在中国的发展,推动我国3R事业和非动物测试发展。替代动物实验进行体外皮肤刺激性检测,更加精准化、人性化。而参与国家标准的制定,也让磐升生物在行业的标准化发展方面掌握更多话语权。